中級通信設備環境知識點精講之鉛酸蓄電池的工作原理
摘要:下面是由希賽小編整理的中級通信設備環境知識點精講之鉛酸蓄電池的工作原理,希望能幫助學友們。具體內容如下
下面是由希賽小編整理的中級通信設備環境知識點精講之鉛酸蓄電池的工作原理,希望能幫助學友們。具體內容如下:
鉛酸蓄電池的工作原理
蓄電池是一種化學電源,構造形式各式各樣,但從原理上講所有的電池都是由正極、負極、電解質、隔離物和容器組成,其中正負兩極的活性物質和電解質起電化反應,對電池產生電流起著主要作用。
在電池內部,正極和負極通過電解質構成電池的內電路,在電池外部接通兩極的導線和負荷構成電池的外電路。
在電極和電解液的接觸面有電極電位產生,不同的兩極活性物質產生不同的電極電位,有著較高電位的電極稱為正極,有著較低電位的電極稱為負極,這樣在正負極之間產生了電位差。當外電路接通時,就有電流從正極綠過外電路流向負極。再由負極經過內電路流向正極,電池向外電路輸送電流的過程稱為電池的放電。
在放電過程中,兩極活性物質逐漸消耗,負極活性物質放出電子而被氧化,正極活性物質吸收從外電路流回的電子而被還原,這樣負極電位逐漸升高。正極電位逐漸降低,兩極間的電位差也就逐漸降低,而且由于電化反應形成新的化合物增加了電池的內阻,使電池輸出電流逐漸減少,直至不能滿足使用要求時,或在外電路兩電極之間端電壓低于一定限度時,電池放電即告終。
電池放電以后,用外來直流電源以適當的反向電流通入,可以使已形成的新化合物還原成為原來的活性物質,而電池又能放電,這種用反向電流使活性物質還原的過程稱為充電。
蓄電池可以反復多次充電、放電,循環使用,使用壽命長,成本較低,能輸出較大的能量,放電時電壓下降很慢。
1.電動勢的產生
鉛蓄電池正極板上的活性物質是二氧化鉛,負極板上的活性物質是海綿狀鉛。在稀硫酸溶液中,由于電化學作用,正負極板與電解液之間分別產生了電極電位,正負兩極間電位差就是蓄電池的電動勢。
負極板上的海綿狀金屬鉛是由二價鉛離子(Pb2+)和電子組成的。稀硫酸在水中被電離為氫離子(H+)和硫酸根離子(S042-)。負極板浸入稀硫酸溶液后,二價鉛離于進入溶液,在極板上留下能夠自由移動的電子,因而負極板帶負電,即產生了電極電位。
同樣,正極板上的二氧化鉛也與稀硫酸作用,產生的四價鉛正離子(Pt)留在極板上,使正極板帶正電,也產生了電極電位。這樣,在電池的正負兩極上便產生了電動勢。
2.放電過程
(1)負極
放電過程中,負極的鉛原子失去兩個電子,變成二價鉛正離子。電解液中的硫酸分子(H2S04)離解為兩個氫離子(H+)和一個硫酸根離子(S042_)。此時二價鉛正離子(Pb2+)與一個硫酸根離子結合成硫酸鉛(PbS04)分子,附著在負極板上。兩個氫離子留在電解液中,參加正極化學反應。負極板失去的電子將通過外電路流入正極。反應式如下:
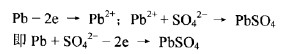
(2)正極
放電開始后,正極上的二氧化鉛與電解液中的水分子作用,生成四價鉛離子(Pb4>)和四個氫氧根離子(0H)。每個四價鉛離子接受負極傳來的兩個電子后生成Pb2’再進入溶液與硫酸根(SO-2)結合成硫酸鉛分子(PbS04)附在正極上,氫氧根離子(OH-)與溶液中氫離子(H+)反應生成水分子。反應式如下:
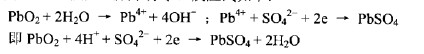
以上兩式相加,就得到鉛蓄電池放電過程中的總反應方程式:

從化學反應式可看出,鉛蓄電池在放電過程中,正負極板上的活性物質都變成了硫酸鉛。電解液中的硫酸不斷消耗,水分子不斷生成,因此,電解液的密度逐漸降低。電解液密度可作為放電終了的標志。
3.充電過程
充電時,外接直流電源的正極與負極分別接蓄電池的正極與負極。當外加電壓高P蓄電池的電動勢時,電子從蓄電池的正極流向負極,從而發生與放電時相反的電化學反應。
(1)負極
蓄電池充電時,負極上的硫酸鉛電離為二價鉛離子(Pb2+)和硫酸根離子(so42-)。二價鉛離子得到兩個電子后,還原為海綿狀鉛,硫酸根離子和電解液中的水分子離解出來的氫離子(H+)結合為硫酸分子(H2S04)。反應式如下:
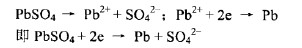
(2)正極
正極上的硫酸鉛電離為二價鉛離子和硫酸根離子。二價鉛離了從外接電源強行奪去兩個電子后,成為四價鉛離子(Pb4+),四價鉛離子與水分子反應,生成二氧化鉛沉積到正極板上。反應式如下:
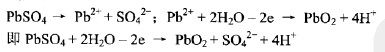
以上兩式相加,可得到鉛蓄電池充電時的電化學反應方程式:
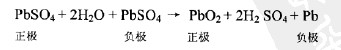
可以看出,正負極板上的硫酸鉛分別變成二氧化鉛和海綿狀鉛,電解液中的水分子不斷消耗,硫酸分子不斷生成,電解液密度不斷升高。因此,電解液密度可以作為充電終了的標志。
蓄電池兩極板上的活性物質完全恢復后,若再繼續充電,則充電電流主要用于分解水。這種反應在充電初期很微弱,但當單體電池端電壓達到2.3V后逐漸增強,過去一般把“2.3V”稱作“發氣點”.莆電池在充電過程中產生的氣體主要是氧氣和氧其中,負極板上有大里氫氣冒出,正極板上有大量氧氣冒出。其化學反應方程式如下:
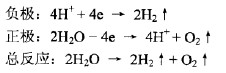
水的分解不僅使電解液減少,而且浪費電能,同時激烈氣泡的沖擊能夠加速活性物質脫落,使蓄電池壽命縮短。因此,充電后期必須減小充電電流,減緩冒氣的劇烈程度,以延長電池的壽命。
相關推薦:
延伸閱讀
- 通信工程師中級動力與環境證書價值有哪些?
- 通信工程師中級動力與環境實務答題技巧
- 通信工程師中級動力與環境備考技巧
- 通信工程師中級動力與環境核心考點
- 通信工程師中級動力與環境報考指南
- 考通信工程師中級動力與環境需要培訓嗎?

通信工程師微信公眾號

通信工程師備考資料免費領取
去領取
距離2026 通信工程師考試
還有- 1
- 4
- 8











 專注在線職業教育25年
專注在線職業教育25年
 掃描二維碼
掃描二維碼
 掃描二維碼
掃描二維碼








